morová hůlka(Yersinia pestis) - druh gramnegativních sporotvorných bakterií, fakultativně anaeroby. Původce dýmějového moru, zápalu plic (pneumonický mor) a septikemického moru.
mor člověka
U lidí je mor charakterizován náhlým zvýšením teploty a malátností, které mohou být doprovázeny bolestmi břicha, nevolností a zvracením. V závislosti na způsobu infekce existují tři hlavní formy moru: Úmrtnost na mor bez léčby se pohybuje od 63 % do 93 %. Při léčbě moderními antibiotiky - přibližně 16%. Rychlá léčba antimikrobiálními látkami, jako jsou aminoglykosidy, fluorochinolony nebo doxycyklin, významně zvyšuje pravděpodobnost příznivého výsledku.
Úmrtnost na mor bez léčby se pohybuje od 63 % do 93 %. Při léčbě moderními antibiotiky - přibližně 16%. Rychlá léčba antimikrobiálními látkami, jako jsou aminoglykosidy, fluorochinolony nebo doxycyklin, významně zvyšuje pravděpodobnost příznivého výsledku. Ve stoletích XIV-XVII v Evropě podle různých odhadů zemřelo na dýmějový mor 50 až 75 milionů lidí. Poslední epidemie moru byla zaregistrována na Madagaskaru v létě 2015.
Mor člověka v USA
Podle zprávy Centra pro kontrolu a prevenci nemocí (CDC) ze dne 25. srpna 2015 bylo ve Spojených státech za období od roku 2001 do roku 2012 zaznamenáno 1 až 17 případů lidské infekce morem (v průměru tři případy ročně ). Mezi 1. 4. 2015 (do 25. 8. 2015) bylo v 6 státech registrováno 11 případů lidského moru (původce Yersinia pestis). 2 případy jsou spojeny s návštěvou Yosemitského národního parku v Kalifornii. Zemřeli 3 pacienti (16, 52 a 79 let). Důvod prudkého nárůstu výskytu moru v roce 2015 ve Spojených státech, jak je uvedeno ve zmíněném vydání, není jasný.Yersinia pestis v MKN-10
Yersinia pestis mezinárodní klasifikace nemocí MKN-10 je uvedena v „I. třídě. Některá infekční a parazitární onemocnění“, v bloku „A20-A28 Některé bakteriální zoonózy“, kde je tříznakový nadpis „A20 Mor“ s dekódováním, že zahrnuje infekci způsobenou Yersinia pestis. Tato rubrika obsahuje čtyřznakové rubriky:
že zahrnuje infekci způsobenou Yersinia pestis. Tato rubrika obsahuje čtyřznakové rubriky: - A20.0 Dýmějový mor
- A20.1 Buněčný kožní mor
- A20.2 Pneumonický mor
- A20.3 Morová meningitida
- A20.7 Septický mor
- A20.8 Jiné formy moru
- A20.9 Mor, blíže neurčený
Změnila malá mutace v Yersinia pestis lidskou historii?
V článku publikovaném v roce 2015 v časopise Nature Communications Dr. D. Zimbler a Dr. W. Lathem z Northwestern University (USA) popsal jediný genetický rys, který objevili Yersinia pestis, která zásadně změnila průběh evoluce mikroorganismu a historii lidstva. V minulosti Yersinia pestis nemohl způsobit plicní mor. Získání jediného genu povrchového proteinu Pla vedlo k transformaci Yersinia pestis z patogenu, který způsobuje střevní infekční onemocnění, na mikroorganismus spojený se vznikem těžkých a smrtelných respiračních infekcí.Více než polovina populace Evropy ve středověku (XIV. století) byla vyhubena morem známým jako černá smrt. Hrůza těchto epidemií zůstala v paměti lidí i po několika staletích a byla zachycena i na plátnech umělců. Dále mor opakovaně navštívil Evropu a vyžádal si lidské životy, i když ne v takovém množství.
V současnosti morová nemoc přetrvává. Ročně se nakazí asi 2 tisíce lidí. Většina z nich zemře. Většina případů infekce je pozorována v severních oblastech Číny a zemích Střední Asie. Podle odborníků dnes neexistují důvody a podmínky pro vznik černé smrti.
Agent moru byl objeven v roce 1894. Ruští vědci při studiu epidemií této nemoci vyvinuli principy vývoje nemoci, její diagnostiky a léčby a byla vytvořena vakcína proti moru.
Příznaky moru závisí na formě onemocnění. Když jsou postiženy plíce, pacienti se stávají vysoce nakažlivými, protože se infekce šíří do prostředí vzdušnými kapkami. U dýmějové formy moru jsou pacienti mírně nakažliví nebo nejsou nakažliví vůbec. V sekretech postižených lymfatických uzlin patogeny chybí, nebo je jich velmi málo.
Léčba moru se stala mnohem účinnější s příchodem moderních antibakteriálních léků. Úmrtnost na mor od té doby klesla na 70 %.
Prevence moru zahrnuje řadu opatření, která omezují šíření infekce.
Mor je akutní infekční zoonotické onemocnění přenášené vektory, které je v zemích SNS spolu s nemocemi jako cholera, tularémie a neštovice považováno za (AI).
Rýže. 1. Obraz "Triumf smrti". Pieter Brueghel.
původce moru
V roce 1878 G. N. Minkh a v roce 1894 A. Yersen a S. Kitazato nezávisle na sobě objevili původce moru. Následně ruští vědci studovali mechanismus rozvoje nemoci, principy diagnostiky a léčby a vytvořili vakcínu proti moru.
- Původcem (Yersinia pestis) je bipolární nepohyblivý kokobacilus, který má jemnou tobolku a nikdy netvoří spor. Schopnost tvořit pouzdro a antifagocytární hlen neumožňuje makrofágům a leukocytům aktivně bojovat s patogenem, v důsledku čehož se rychle množí v orgánech a tkáních lidí a zvířat a šíří se krevním řečištěm a lymfatickým traktem po celém tělo.
- Morové patogeny produkují exotoxiny a endotoxiny. Exo- a endotoxiny jsou obsaženy v tělech a pouzdrech bakterií.
- Enzymy bakteriální agrese (hyaluronidáza, koaguláza, fibrinolysin, hemolysin) usnadňují jejich průnik do organismu. Tyčinka je schopna proniknout i přes neporušenou pokožku.
- V zemi neztrácí morový bacil svou životaschopnost až několik měsíců. V mrtvolách zvířat a hlodavců přežívá až jeden měsíc.
- Bakterie jsou odolné vůči nízkým teplotám a mrazu.
- Morové patogeny jsou citlivé na vysoké teploty, kyselé prostředí a sluneční záření, které je zahubí za pouhé 2 až 3 hodiny.
- Až 30 dní zůstávají patogeny v hnisu, až 3 měsíce - v mléce, až 50 dní - ve vodě.
- Dezinfekční prostředky zničí morový bacil během pár minut.
- Morové patogeny způsobují onemocnění u 250 druhů zvířat. Většina z nich jsou hlodavci. K onemocnění jsou náchylní velbloudi, lišky, kočky a další zvířata.

Rýže. 2. Na fotografii bakterie moru - bakterie způsobující mor - Yersinia pestis.
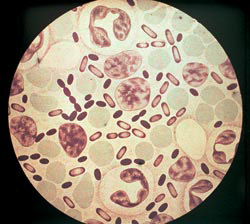
Rýže. 3. Na fotografii původci moru. Intenzita barvení anilinovými barvivy je největší na pólech bakterií.
php?post=4145&action=edit#
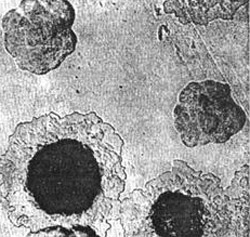
Rýže. 4. Na fotografii patogeny moru - růst na hustém médiu kolonie. Kolonie zpočátku vypadají jako rozbité sklo. Dále je jejich střední část zhutněná a obvod připomíná krajku.
Epidemiologie
Zásobník infekce
K morovému bacilu jsou snadno náchylní hlodavci (tarbagani, svišti, pískomilové, sysli, krysy a myši domácí) a zvířata (velbloudi, kočky, lišky, zajíci, ježci atd.). Z laboratorních zvířat jsou k infekci náchylné bílé myši, morčata, králíci a opice.
Psi mor nikdy nedostanou, ale přenášejí patogen kousnutím krev sajícího hmyzu – blechami. Zvíře, které zemřelo na nemoc, přestává být zdrojem infekce. Pokud hlodavci infikovaní morovými bacily upadnou do hibernace, pak u nich nemoc získá latentní průběh a po hibernaci se opět stanou distributory patogenů. Celkem se jedná až o 250 druhů zvířat, která jsou nemocná, a proto jsou zdrojem a rezervoárem nákazy.

Rýže. 5. Hlodavci jsou rezervoárem a zdrojem patogenu moru.
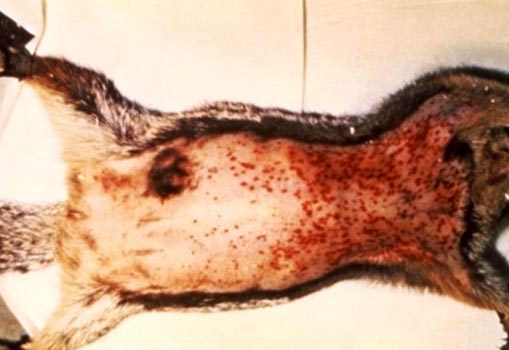
Rýže. 6. Fotografie ukazuje známky moru u hlodavců: zvětšené lymfatické uzliny a mnohočetné krvácení pod kůží.

Rýže. 7. Na fotografii malý jerboa je přenašečem moru ve střední Asii.

Rýže. 8. Na fotografii je černý potkan přenašečem nejen moru, ale i leptospirózy, leishmaniózy, salmonelózy, trichinelózy atd.
Způsoby infekce
- Hlavní cestou přenosu patogenů je kousnutí blechami (přenosná cesta).
- Infekce se může dostat do lidského těla při práci s nemocnými zvířaty: porážka, stahování z kůže a řezání (kontaktní cesta).
- Patogeny se mohou do lidského těla dostat s kontaminovanými potravinami, v důsledku jejich nedostatečné tepelné úpravy.
- Od pacienta s plicní formou moru se infekce šíří vzdušnými kapénkami.

Rýže. 9. Na fotografii je blecha na lidské kůži.

Rýže. 10. Na fotce moment blešího kousnutí.
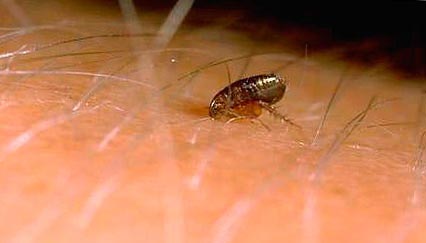
Rýže. 11. Okamžik blešího kousnutí.
Patogenní vektory
- Přenašeči patogenů jsou blechy (v přírodě existuje více než 100 druhů tohoto hmyzu členovců),
- Přenašeči patogenů jsou některé druhy klíšťat.
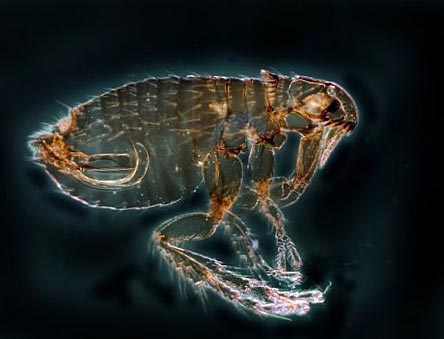
Rýže. 12. Na fotografii je hlavním přenašečem moru blecha. V přírodě existuje více než 100 druhů tohoto hmyzu.

Rýže. 13. Na fotografii je blecha gopher hlavním přenašečem moru.
Jak dochází k infekci
K infekci dochází kousnutím hmyzem a třením jeho výkalů a střevního obsahu během regurgitace během krmení. Když se bakterie množí ve střevní trubici blechy, pod vlivem koagulázy (enzymu vylučovaného patogeny) se vytvoří „zástrčka“, která brání lidské krvi vstoupit do jejího těla. V důsledku toho blecha regurgituje sraženinu na kůži kousnutého. Infikované blechy zůstávají vysoce infekční po dobu 7 týdnů až 1 roku.

Rýže. 14. Na fotografii je bleší kousnutí pulitické podráždění.
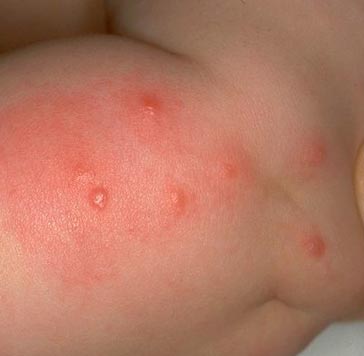
Rýže. 15. Na fotografii je charakteristická série bleších kousnutí.

Rýže. 16. Pohled na bérci s bleším kousnutím.
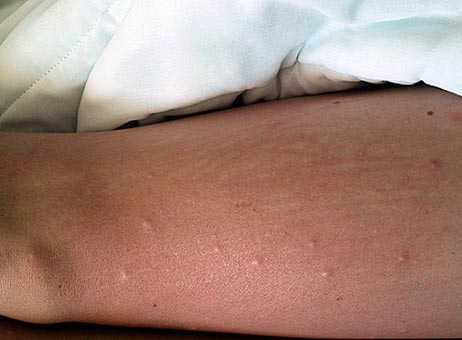
Rýže. 17. Pohled na stehno s bleším kousnutím.
Člověk jako zdroj nákazy
- Když jsou postiženy plíce, pacienti se stávají vysoce nakažlivými. Infekce se šíří do prostředí vzdušnými kapénkami.
- U dýmějové formy moru jsou pacienti mírně nakažliví nebo nejsou nakažliví vůbec. V sekretech postižených lymfatických uzlin patogeny chybí, nebo je jich velmi málo.
Mechanismy rozvoje moru
Schopnost morového bacilu tvořit pouzdro a antifagocytární hlen neumožňuje makrofágům a leukocytům s ním aktivně bojovat, v důsledku čehož se patogen rychle množí v orgánech a tkáních lidí a zvířat.
- Původci moru přes poškozenou kůži a dále podél lymfatického traktu pronikají do lymfatických uzlin, které se zanítí a tvoří konglomeráty (buboy). V místě kousnutí hmyzem vzniká zánět.
- Průnik patogenu do krevního řečiště a jeho masivní rozmnožování vede k rozvoji bakteriální sepse.
- Od pacienta s plicní formou moru se infekce šíří vzdušnými kapénkami. Bakterie pronikají do alveol a způsobují těžký zápal plic.
- V reakci na masivní množení bakterií produkuje tělo pacienta obrovské množství zánětlivých mediátorů. Rozvíjející se syndrom diseminované intravaskulární koagulace(DIC), při které jsou postiženy všechny vnitřní orgány. Zvláštní nebezpečí pro tělo představují krvácení do srdečního svalu a nadledvinek. Rozvinutý infekčně-toxický šok způsobí smrt pacienta.

Rýže. 18. Na fotografii je dýmějový mor. Typické zvětšení lymfatické uzliny v podpaží.
příznaky moru
Onemocnění se projevuje po průniku patogenu do těla po dobu 3-6 dnů (zřídka, ale vyskytly se případy manifestace onemocnění 9. den). Když se infekce dostane do krevního řečiště, inkubační doba je několik hodin.
Klinický obraz počátečního období
- Akutní nástup, velké množství teploty a zimnice.
- Myalgie (bolest svalů).
- Bolestivá žízeň.
- Silný projev slabosti.
- Rychlý rozvoj psychomotorické agitace („šílenec“ se nazývá takoví pacienti). Na obličeji se objeví maska hrůzy („morová maska“). Méně často je zaznamenána letargie a apatie.
- Obličej se stává hyperemickým a nafouknutým.
- Jazyk je hustě potažený bílou barvou ("křídový jazyk").
- Na kůži se objeví mnohočetné krvácení.
- Výrazně zvýšená srdeční frekvence. Objeví se arytmie. Krevní tlak klesá.
- Dýchání se stává mělkým a rychlým (tachypnoe).
- Množství vyloučené moči se prudce sníží. Rozvíjí se anurie (úplný nedostatek výdeje moči).

Rýže. 19. Na fotografii asistenci morovému pacientovi poskytují lékaři oblečení v protimorových oblecích.
Formy moru
Lokální formy onemocnění
Forma kůže
V místě blešího kousnutí nebo kontaktu s infikovaným zvířetem se na kůži objeví papule, která rychle ulceruje. Pak se objeví černý strup a jizva. Nejčastěji jsou kožní projevy prvními příznaky hrozivějších projevů moru.
bubonická forma
Nejčastější projev onemocnění. V blízkosti místa kousnutí hmyzem (inguinální, axilární, cervikální) se objevuje zvýšení lymfatických uzlin. Častěji se zanítí jedna lymfatická uzlina, méně často - několik. Při zánětu více lymfatických uzlin najednou se tvoří bolestivé bubo. Zpočátku je lymfatická uzlina pevné konzistence, bolestivá při palpaci. Postupně měkne a získává pastovitou konzistenci. Dále se lymfatická uzlina buď upraví, nebo ulceruje a skleróza. Z postižené lymfatické uzliny se infekce může dostat do krevního oběhu s následným rozvojem bakteriální sepse. Akutní fáze bubonické formy moru trvá asi týden.

Rýže. 20. Na fotografii postižené krční lymfatické uzliny (buboes). Mnohočetné krvácení do kůže.
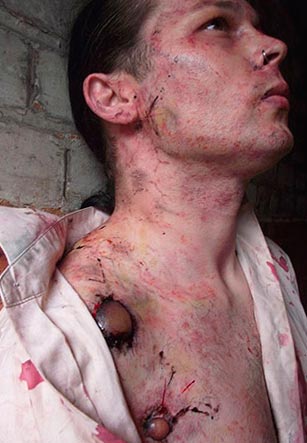
Rýže. 21. Na fotografii je bubonická forma moru léze krčních lymfatických uzlin. Mnohočetné krvácení do kůže.

Rýže. 22. Fotografie ukazuje bubonickou formu moru.
Běžné (zobecněné) formy
Když se patogen dostane do krevního oběhu, vyvinou se rozšířené (generalizované) formy moru.
Primární septická forma
Pokud se infekce, která obchází lymfatické uzliny, okamžitě dostane do krevního oběhu, pak se vyvine primární septická forma onemocnění. Intoxikace se vyvíjí rychlostí blesku. Při masivní reprodukci patogenů v těle pacienta vzniká obrovské množství zánětlivých mediátorů. To vede k rozvoji syndromu diseminované intravaskulární koagulace (DIC), při kterém jsou postiženy všechny vnitřní orgány. Zvláštní nebezpečí pro tělo představují krvácení do srdečního svalu a nadledvinek. Rozvinutý infekčně-toxický šok způsobí smrt pacienta.
Sekundární septická forma onemocnění
Když se infekce rozšíří mimo postižené lymfatické uzliny a patogeny se dostanou do krevního řečiště, vzniká infekční sepse, která se projevuje prudkým zhoršením stavu pacienta, zvýšenými příznaky intoxikace a rozvojem DIC. Rozvinutý infekčně-toxický šok způsobí smrt pacienta.

Rýže. 23. Na fotografii je septická forma moru následky DIC.

Rýže. 24. Na fotografii je septická forma moru následky DIC.
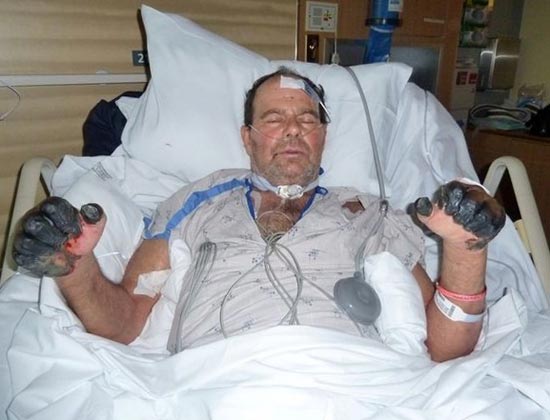
Rýže. 25. 59letý Paul Gaylord (s bydlištěm v Portlandu, Oregon, USA). Bakterie moru se do jeho těla dostala od zatoulané kočky. V důsledku rozvinuté sekundární septické formy onemocnění mu byly amputovány prsty na rukou a nohou.
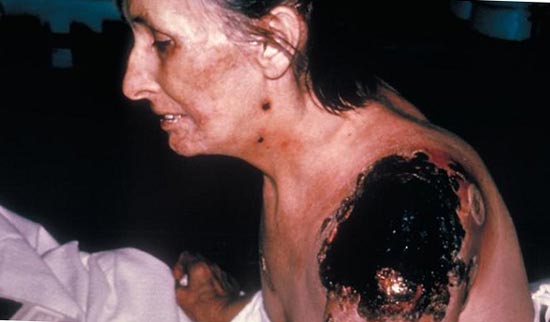
Rýže. 26. Důsledky DIC.
Externě diseminované formy onemocnění
Primární plicní forma
Pneumonický mor je nejtěžší a nejnebezpečnější formou onemocnění. Infekce proniká do alveol vzdušnými kapénkami. Porážka plicní tkáně je doprovázena kašlem a dušností. Zvýšení tělesné teploty pokračuje silnou zimnicí. Sputum na začátku onemocnění je husté a průhledné (sklovité), poté se stává tekutým a pěnivým, s příměsí krve. Vzácná data fyzikálního vyšetření neodpovídají závažnosti onemocnění. DIC se vyvíjí. Postiženy jsou vnitřní orgány. Zvláštní nebezpečí pro tělo představují krvácení do srdečního svalu a nadledvinek. Smrt pacienta nastává v důsledku infekčně toxického šoku.
Když jsou postiženy plíce, pacienti se stávají vysoce nakažlivými. Vytvářejí kolem sebe ohnisko obzvláště nebezpečné infekční choroby.
Sekundární plicní forma
Jde o extrémně nebezpečnou a závažnou formu onemocnění. Patogeny pronikají do plicní tkáně z postižených lymfatických uzlin nebo krevním řečištěm při bakteriální sepsi. Klinika a výsledek onemocnění, jako u primární plicní formy.
střevní forma
Existence této formy onemocnění je kontroverzní. Předpokládá se, že k infekci dochází při použití infikovaných produktů. Zpočátku se na pozadí syndromu intoxikace objevují bolesti břicha a zvracení. Pak se připojí průjem a četná nutkání (tenesmus). Stolice je hojná, slizničně krvavá.
Rýže. 27. Fotografie protimorového obleku - speciální vybavení pro zdravotnické pracovníky při likvidaci ohniska zvlášť nebezpečného infekčního onemocnění.
Laboratorní diagnostika moru
Základem pro diagnostiku moru je rychlé odhalení morového bacila. Nejprve se provádí bakterioskopie nátěrů. Dále se izoluje kultura patogenu, která infikuje experimentální zvířata.
Materiálem pro studium je obsah bubo, sputum, krev, výkaly, kousky tkání z orgánů mrtvých a mrtvoly zvířat.
Bakterioskopie
Původcem moru (Yersinia pestis) je tyčinkovitý bipolární kokobacilus. Analýza pro detekci morového bacila přímou bakterioskopií je nejjednodušší a nejrychlejší způsob. Čekací doba na výsledek není delší než 2 hodiny.
Plodiny biologického materiálu
Kultura patogenu moru se izoluje ve specializovaných režimových laboratořích určených pro práci. Doba růstu patogenní kultury je dva dny. Dále se provede test citlivosti na antibiotika.
Sérologické metody
Použití sérologických metod umožňuje stanovit přítomnost a růst protilátek v krevním séru pacienta proti patogenu moru. Doba pro obdržení výsledku je 7 dní.

Rýže. 28. Diagnostika moru se provádí v laboratořích se zvláštním režimem.

Rýže. 29. Na fotografii původci moru. Fluorescenční mikroskopie.

Rýže. 30. Na fotografii kultura Yersinia pestis.
Morová imunita
Protilátky proti zavlečení patogenu moru se tvoří v poměrně pozdní fázi vývoje onemocnění. Imunita po nemoci není dlouhá a není napjatá. Opakují se případy onemocnění, které postupují stejně tvrdě jako první.
léčba moru
Před zahájením léčby je pacient hospitalizován v samostatném boxu. Zdravotnický personál obsluhující pacienta je oblečen do speciálního protimorového obleku.
Antibakteriální úprava
Antibakteriální léčba začíná při prvních příznacích a projevech onemocnění. Z antibiotik jsou preferovány antibakteriální léky skupiny aminoglykosidů (streptomycin), skupiny tetracyklinů (vibromycin, morfocyklin), skupiny fluorochinolonů (ciprofloxacin), skupiny ansamycinu (rifampicin). V léčbě kožní formy onemocnění se osvědčilo antibiotikum amfenikolové skupiny (kortrimoxazol). U septických forem onemocnění se doporučuje kombinace antibiotik. Průběh antibiotické terapie je minimálně 7-10 dní.
Léčba zaměřená na různé fáze vývoje patologického procesu
Cílem patogenetické terapie je snížení syndromu intoxikace odstraněním toxinů z krve pacienta.
- Je ukázáno zavedení čerstvé zmrazené plazmy, proteinových přípravků, rheopolyglucinu a dalších léků v kombinaci s forsírovanou diurézou.
- Zlepšení mikrocirkulace je dosaženo použitím trentalu v kombinaci se salcoserylem nebo pikamilonem.
- S rozvojem krvácení se okamžitě provádí plazmaferéza, aby se zastavil syndrom diseminované intravaskulární koagulace.
- Při poklesu tlaku je předepsán dopamid. Tento stav ukazuje na generalizaci a rozvoj sepse.
Symptomatická léčba
Symptomatická léčba je zaměřena na potlačení a odstranění projevů (příznaků) moru a v důsledku toho na zmírnění utrpení nemocného. Je zaměřena na odstranění bolesti, kašle, dušnosti, dušení, tachykardie atd.
Pacient je považován za zdravého, pokud vymizely všechny příznaky onemocnění a byly získány 3 negativní výsledky bakteriologického vyšetření.
Protiepidemická opatření
Identifikace pacienta s morem je signálem pro okamžité jednání, mezi které patří:
- provádění karanténních opatření;
- okamžitá izolace pacienta a preventivní antibakteriální léčba ošetřovatelů;
- dezinfekce v ohnisku onemocnění;
- očkování osob v kontaktu s pacientem.
Po očkování vakcínou proti moru imunita přetrvává rok. Přeočkováno po 6 měsících. osoby ohrožené reinfekcí: pastevci, myslivci, pracovníci v zemědělství a zaměstnanci protimorových institucí.

Rýže. 31. Na fotografii je lékařský tým oblečený v protimorových oblecích.
Prognóza onemocnění
Prognóza moru závisí na následujících faktorech:
- formy onemocnění
- včasnost zahájení léčby,
- dostupnost celého arzenálu drogové i nedrogové léčby.
Nejpříznivější prognóza u pacientů s lézemi lymfatických uzlin. Úmrtnost v této formě onemocnění dosahuje 5%. U septické formy onemocnění dosahuje úmrtnost 95 %.
Mor je a i při použití všech potřebných léků a manipulací končí nemoc často smrtí pacienta. Morové patogeny v přírodě neustále cirkulují a nelze je zcela zničit a ovládat. Příznaky moru jsou různé a závisí na formě onemocnění. Dýmějová forma moru je nejčastější.
Články sekce "Zvlášť nebezpečné infekce"Nejoblíbenější
Mor (pestis) je akutní infekční onemocnění, které se projevuje celkovou intoxikací a charakteristickými zánětlivými procesy v lymfatických uzlinách, plicích, kůži a dalších orgánech. Mor patří do skupiny tzv. zvláště nebezpečných (karanténních) infekcí s. Zlikvidován v SSSR.
Etiologie. Původcem je morový bacil se zaoblenými konci, uprostřed oteklý, v důsledku čehož má vejčitý tvar. Malováno běžnými anilinovými barvami; střední část je zbarvena bleději (bipolární barvení). Odolnost vůči okolním vlivům je nízká. Sušení, sluneční záření, konkurence hnilobných mikrobů ji rychle zničí; varem zabíjí do 1 minuty. Hůl dobře snáší nízké teploty. Mikrob může přežívat dlouhou dobu na prádle, oblečení kontaminovaném sputem, hnisem, krví; je dlouhodobě skladován ve vodě, na potravinářských výrobcích. V mrtvolách hlodavců, pokud nedojde k procesu rozkladu (v zimě), může hůl zůstat životaschopná po dobu 4-5 měsíců. Roztoky 5% lysolu a 5-10% kyseliny karbolové zabíjejí bacil moru za 5-10 minut a roztok sublimátu 1:1000 za 1-2 minuty.
Epidemiologie. Strážcem nákazy v přírodě jsou volně žijící hlodavci (syli, svišti, pískomilové). Dostatečná hustota a kontinuita kolonií hlodavců, velké množství blech - infekcí, schopnost hibernujících syslů a svišťů přenášet infekci v latentní formě zajišťuje nepřetržitou cirkulaci patogena moru mezi těmito hlodavci. Velmi náchylné k moru jsou také domácí potkani, myši domácí, hraboši, stepní lumíci a další druhy myším podobným. Tito hlodavci nedokážou zajistit nekonečně dlouhé uložení patogenu moru v přírodě. To ale nevylučuje možnost vzniku mocných (viz) mezi myšími podobnými, zejména s tzv. myšími neštěstími, což s sebou nese zase těžké mezi lidmi. Pro udržení dlouhodobé epizootiky mezi hlodavci je nezbytná vysoká hustota a velké množství blech na nich. Takové podmínky se obvykle vytvářejí pouze v jižních zeměpisných šířkách, například v zemích Středního a Dálného východu, kde morovou infekci mezi lidmi obvykle šíří synantropní krysy. Velký význam má velbloud náchylný k moru. V minulosti mezi lidmi často propukla morová epidemie spojená s nuceným zabíjením nemocných velbloudů. Lišky, šakali a fretky náchylné k moru mají malý praktický význam. Infekce mezi hlodavci se šíří především přenosnou cestou (prostřednictvím blech).
Šíření moru mezi lidmi je možné přenosnými, vzdušnými a kontaktními cestami domácností. Výskyt prvních případů moru u lidí vždy začíná dýmějovými formami v důsledku přenosného nebo kontaktního mechanismu přenosu infekce (bleší kousnutí, stažení kůže nemocného hlodavce, poražení mršiny velblouda při porážce nemocného zvířete atd.). ). V budoucnu je vývoj nemocí určován jinými přenosovými mechanismy: prostřednictvím infikovaných předmětů pro domácnost a vody. Pokud je bubonická forma moru komplikovaná sekundárním morem, pak nemocný rozptyluje infekci kašlem, mluvením. Vzdušná cesta infekce s sebou nese vznik primárních plicních forem moru, při kterých pacienti masivně infikují okolí.
Patogeneze a patologická anatomie. Místem vstupní brány infekce při moru u člověka může být kůže, sliznice dýchacích cest, spojivky, méně často dochází k infekci přes. Podle toho se rozlišuje kožní forma moru, která se v důsledku rozvoje regionálního bubo brzy změní na kožní bubonickou. Kožní forma je poměrně vzácná (do 3–5 %). Častěji je pozorována bubonická forma moru, u které je bubo (zánět lymfatické uzliny) povinným příznakem. Původce moru je proudem lymfy přiveden do uzliny a způsobuje zánět. Primární buboes se liší od sekundárních buboes, které vznikají hematogenně (krví) obvykle později. Hematogenní infekce se může dostat do plic (sekundární plicní mor), do mozku (možná meningitida) a v některých případech vést k (sekundární septikemický mor). U primárního plicního moru má poškození plic častěji ohniskovou povahu. V těžkých případech zánětlivý proces zachycuje celý lalok nebo několik laloků, charakteristický je serózně-hemoragický. Střevní forma je velmi vzácná.
Mor (pestis) je akutní infekční onemocnění ze skupiny zoonóz, projevující se rozvojem akutní intoxikace a zánětlivých procesů v lymfatických uzlinách, plicích a dalších orgánech.
V současnosti je mor hlášen v Asii, Africe, Severní a převážně Jižní Americe. Evropa a Austrálie jsou osvobozeny od moru.
Etiologie
Patogen H, - Bacterium pestis, Pasteurella pestis - polymorfní tyčinka dlouhá 1-3 mikrony a široká 0,3-0,7 mikronu. Konce bakterií jsou zaoblené a střed je mírně oteklý, v důsledku čehož mají vejčitý (vejčitý) tvar. Snadno se barví anilinovými barvivy, gramnegativní. Při barvení je střední část mikrobiálních buněk obarvena bleději než jejich konce (bipolární barvení), zejména při barvení methylenovou modří a podle Romanovského-Giemsy (obr. 1). Bakterie vejčitého tvaru s výrazným bipolárním zbarvením převládají ve stěrech z punktátů bubo, z krve a orgánů čerstvých lidských a zvířecích mrtvol.
Rýže. 1. Bipolární obarvené tyčinky moru ze sleziny morčete (X1200).
Rýže. 2. Dvoudenní kolonie morového mikroba na agaru (X40).
Změněné formy bakterií (kuličky, ztluštělá vlákna) se nacházejí ve stěrech z hnisavých bubů, z orgánů rozpadlých mrtvol a při růstu na agaru s přídavkem soli. Barvené nátěry z 24-48hodinové agarové kultury ukazují krátké tyčinky (typy koko) a tyčinky umístěné jednotlivě a ve skupinách. Mezi nimi jsou dlouhé zkroucené
závity a kulové (involuční) formy. V nátěrech z bujónové kultury - tyčinky různých délek, uspořádané ve formě řetězů.
Bakterie moru nemají aktivní pohyblivost, netvoří spory, mají pouzdro. Na umělých živných půdách je tvorba kapsle usnadněna pěstováním při t ° 37 °, vlhkém a mírně kyselém prostředí, přidáním krve, glykolu do média a pěstováním v atmosféře obsahující 20-25 % oxidu uhličitého.
Původcem moru je fakultativní anaerob. Dobře roste na běžných živných půdách s optimálním pH média rovným 6,9-7,2 při t ° 25-30 °.
Obvykle roste ve tvaru R, někdy ve tvaru S. Ve tvaru R jsou kolonie drsné, konvexní, s hnědým středem, obklopené na obvodu krajkovým okrajem (obr. 2); ve tvaru S - hladká, průhledná, bez krajkové zóny. Virulentní morové mikroby izolované z nemocných hlodavců a lidí, stejně jako z blech, rostou v R-formě.
Bakterie moru nezkapalňují želatinu a sraženou syrovátku; fermentovat za vzniku kyselé glukózy, maltózy, mannitolu a arabinózy, nefermentovat laktózu, sacharózu a rhamnózu. Ve vztahu ke glycerolu se rozlišují dvě odrůdy morového mikroba: glycerin-pozitivní a glycerin-negativní.
Původce moru dobře snáší nízké teploty, ale je velmi citlivý na teplo; při t ° 58 ° zemře do 30 minut a při bodu varu - během 1-5 minut. Citlivý na přímé sluneční světlo. Není odolný vůči působení dezinfekčních prostředků: 3-5% roztok kyseliny karbolové, roztoky lysolu, chloraminu, bělidla, ethylalkoholu jej zabijí během 1-10 minut. V proteinovém prostředí (krvavé sputum, krev atd.) mohou morové mikroby, chráněné před světlem a vysycháním, vydržet až 10-15 dní i více a jsou také odolnější vůči dezinfekčním prostředkům. Po dlouhou dobu (3-5 měsíců) zůstávají v těle blech. V objektech životního prostředí kontaminovaných jinou mikroflórou rychle umírají. Citlivý na antibiotika (streptomycin, tetracykliny atd.).
Morová hůlka(lat. Yersinia pestis) je druh gramnegativních bakterií z čeledi Enterobacteriaceae. Infekční agens dýmějového moru, může také způsobit morový zápal plic a septikemický mor. Všechny tři formy jsou zodpovědné za vysokou úmrtnost při epidemiích, které se v dějinách lidstva odehrály, jako je „Justiniánův mor“ (100 milionů obětí) a „Černá smrt“, která – smrt třetiny populace Evropa mezi 1347 a 1353 lety.
Role Yersinia pestis diskutované v Černé smrti. Někteří tvrdí, že černá smrt se rozšířila příliš rychle na to, aby byla způsobena Yersinia pestis. DNA této bakterie byla nalezena v zubech těch, kteří zemřeli na černou smrt, zatímco testování středověkých pozůstatků lidí, kteří zemřeli z jiných příčin, nepřineslo pozitivní reakci. Yersinia pestis. To dokazuje Yersinia pestis je přinejmenším průvodním faktorem některých (možná ne všech) evropských morových epidemií. Je možné, že selekce morem mohla ovlivnit patogenitu bakterie vyhubením jedinců, kteří jsou k ní nejvíce náchylní.
Rod Yersinia Gram-negativní, bipolární kokobacily. Stejně jako ostatní zástupci Enterobacteriaceae mají enzymatický metabolismus. Y. pestis produkuje antifagocytární hlen. Bakterie, která je v kultuře mobilní, se stane nehybnou, když vstoupí do těla savce.
Příběh
Y. pestis byl objeven v roce 1894 švýcarsko-francouzským lékařem a bakteriologem Pasteurova institutu Alexandrem Yersinem během morové epidemie v Hongkongu. Yersen byl zastáncem Pasteurovy školy. V Německu vyškolený japonský bakteriolog Kitasato Shibasaburo, který praktikoval Kochovu metodu, se také v této době podílel na hledání agenta, který je původcem moru. Byl to však Yersin, kdo ve skutečnosti mor spojil s Y. pestis. Po dlouhou dobu byl původce moru připisován rodu Bakterie, později - do rodu Pasteurella. V roce 1967 byl na počest Alexandra Yersina přejmenován rod bakterií, do kterého původce moru patřil.
V důsledku srovnání starověkých kmenů genů Yersinia pestis a jeho pravděpodobného předka Yersinia pseudotuberculosis(bacil pseudotuberculosis) bylo zjištěno, že Yersinia pestis zmutoval z relativně neškodného mikroorganismu asi před 10 000 lety. Ukázalo se, že život v půdě Y. pseudotuberculosis, který způsobuje mírné onemocnění gastrointestinálního traktu, pak získal několik genů, které mu umožnily proniknout do lidských plic. Dále došlo k jediné aminokyselinové změně v klíčovém genu Pla, v důsledku čehož byl mikroorganismus schopen zvýšenou silou rozkládat proteinové molekuly v plicích a množit se po celém těle lymfatickým systémem. Vědci mají podezření, že morový bacil si vypůjčil gen Pla od jiného mikroba v důsledku horizontální výměny genů. To potvrzují studie dánských a britských vědců, kteří provedli studii molekul DNA extrahovaných ze zubů 101 lidí z doby bronzové nalezených v Eurasii (od Polska po Sibiř). Stopy bakterií Y. pestis nalezený v DNA sedmi, až 5783 let starých, zatímco šest z těchto vzorků postrádalo ymt „gen virulence“ a mutace v „aktivačním genu“ pla. Později, na přelomu druhého a prvního tisíciletí př. n. l., vlivem demografických podmínek, vyjádřených nárůstem populační hustoty, vznikla smrtelnější „bubonická“ mutace bakterie.
Jsou známy tři biovary bakterií; věří se, že každá odpovídá jedné z historických morových pandemií. Biovar antikva považován za odpovědného za Justiniánův mor. Není známo, zda tento biovar byl příčinou dřívějších menších epidemií, nebo se v těchto případech vůbec nejednalo o morové epidemie. Biovar medievalis věřil být spojován s černou smrtí. Biovar orientalis spojené s třetí pandemií a nejmodernějšími epidemiemi moru.
Patogenita a imunita
patogenita Yersinia pestis sestává ze dvou antifagocytárních antigenů tzv F1 a vw, oba jsou nezbytné pro virulenci. Tyto antigeny jsou produkovány bakterií při 37 °C. Kromě, Y. pestis přežívá a produkuje antigeny F1 a VW uvnitř krevních buněk, jako jsou monocyty, s výjimkou polymorfonukleárních neutrofilních granulocytů.
Před časem byla v USA k dispozici formalinem inaktivovaná vakcína pro dospělé s vysokým rizikem infekce, ale poté byl prodej na pokyn FDA, speciální agentury Ministerstva zdravotnictví USA, kvůli nízké účinnosti a pravděpodobnost vážného zánětu. V genetickém inženýrství existují slibné experimenty k vytvoření vakcíny založené na antigenech F1 a VW, ačkoli bakterie postrádající antigen F1 si zachovávají dostatečnou virulenci a antigeny V jsou dostatečně variabilní, takže vakcinace založená na těchto antigenech nemusí poskytnout dostatečnou ochranu.
V Rusku je dostupná živá vakcína založená na nevirulentním kmeni moru.
Očkování nechrání před plicním morem. Během epidemie v letech 1910-1911 použití morových sér (Khavkinova lymfa a Yersenovo sérum) pouze prodloužilo průběh nemoci na několik dní, ale nezachránilo život žádnému pacientovi. Následně bylo vědcům konečně jasné, že humorální imunita při aerogenní infekci patogenem moru nevadí.
Genom
K dispozici jsou kompletní genetické sekvence pro různé bakteriální poddruhy: kmen KIM (z biovaru Medievalis), kmen CO92 (z biovaru Orientalis získaný z klinického izolátoru v USA), kmen Antiqua, Nepal516, Pestoides F. Chromozomy kmene KIM se skládají z 4 600 755 párů bází, v kmeni CO92 - 4 653 728 párů bází. Jako související Y. pseudotuberculosis a Y. enterocolitica, bakterie Y. pestis obsahuje plazmidy pCD1. Kromě toho obsahuje také plazmidy pPCP1 a pMT1 nenachází se u jiných druhů rodu Yersinia. Vyjmenované plazmidy a ostrov patogenity pojmenovány HPI, kódují proteiny, které jsou příčinou patogenity bakterie. Tyto faktory virulence jsou mimo jiné nutné pro bakteriální adhezi a injekci proteinů do hostitelské buňky, bakteriální invazi do hostitelské buňky, zachycení a vazbu železa extrahovaného z erytrocytů.
Léčba
Od roku 1947 tradiční prostředek prvního stupně léčby pro Y. pestis byly streptomycin, chloramfenikol nebo tetracyklin. Existují také důkazy o pozitivním výsledku při použití doxycyklinu nebo gentamicinu.
Je třeba poznamenat, že izolované kmeny jsou rezistentní vůči jednomu nebo dvěma agens uvedeným výše a léčba by měla být pokud možno založena na jejich citlivosti na antibiotika. U některých pacientů samotná léčba antibiotiky nestačí a může být nutná podpora oběhu, dýchání nebo ledvin.
Role Yersinia pestis diskutované v Černé smrti. Někteří tvrdí, že černá smrt se rozšířila příliš rychle na to, aby byla způsobena Yersinia pestis. DNA této bakterie byla nalezena v zubech těch, kteří zemřeli na černou smrt, zatímco testování středověkých pozůstatků lidí, kteří zemřeli z jiných příčin, nepřineslo pozitivní reakci. Yersinia pestis. To dokazuje Yersinia pestis je přinejmenším průvodním faktorem některých (možná ne všech) evropských morových epidemií. Je možné, že selekce morem mohla ovlivnit patogenitu bakterie vyhubením jedinců, kteří jsou k ní nejvíce náchylní.
V Rusku je dostupná živá vakcína založená na nevirulentním kmeni moru.
Genom
K dispozici jsou kompletní genetické sekvence pro různé poddruhy bakterie: kmen KIM (z biovaru Medievalis), kmen CO92 (z biovaru Orientalis, získaný z klinického izolátoru v USA), kmen Antiqua, Nepal516, Pestoides F. Chromozomy kmene KIM se skládají 4 600 755 párů bází, v kmeni C092 - 4 653 728 párů bází. Jako související Y. pseudotuberculosis a Y. enterocolitica, bakterie Y. pestis obsahuje plazmidy pCD1. Kromě toho obsahuje také plazmidy pPCP1 a pMT1 nenachází se u jiných druhů rodu Yersinia. Vyjmenované plazmidy a ostrov patogenity, pojmenovaný HPI, kódují proteiny, které jsou příčinou patogenity bakterie. Tyto faktory virulence jsou mimo jiné nutné pro bakteriální adhezi a injekci proteinů do hostitelské buňky, bakteriální invazi do hostitelské buňky, zachycení a vazbu železa extrahovaného z erytrocytů.
Léčba
Od roku 1947 tradiční prostředek prvního stupně léčby pro Y. pestis byly streptomycin, chloramfenikol nebo tetracyklin. Existují také důkazy o pozitivním výsledku z použití doxycyklinu nebo gentamicinu.
Je třeba poznamenat, že izolované kmeny jsou rezistentní vůči jednomu nebo dvěma agens uvedeným výše a léčba by měla být pokud možno založena na jejich citlivosti na antibiotika. U některých pacientů samotná léčba antibiotiky nestačí a může být nutná podpora oběhu, dýchání nebo ledvin.
Napište recenzi na článek "Morová hůlka"
Poznámky
- Collins FM. Pasteurella, Yersinia a Francisella. V: Barronova lékařská mikrobiologie (Barron S a kol , eds.). - 4. vyd.. - Univ of Texas Medical Branch, 1996. - ISBN.
- - v článku publikovaném v časopise "Knowledge-Power" č. 2 za rok 2002 jsou uvedeny úvahy, které kritizují spojení bakterie s morem.
- Drancourt M; Aboudharam G; Signolidagger M; Dutourdagger O; Raoult D. (1998). "". PNAS 95 (21): 12637–12640.
- Drancourt M; Raoult D. (2002). "". Infikují mikroby. 4 : 105–9.
- . Lenta.ru. Staženo 23-10=2015.
- Daniel L. Zimbler, Jay A. Schroeder, Justin L. Eddy & Wyndham W. Lathem.. nature.com. Staženo 13-02=2016.
- . Lenta.ru. Staženo 23-10=2015.
- Simon Rasmussen.. cell.com. Staženo 13-02=2016.
- Salyers AA, Whitt DD. Bakteriální patogeneze: Molekulární přístup. - 2. vyd.. - ASM Press, 2002. - ISBN pp207-12.
- Welkos S a kol.. (2002). "". Vakcína 20 : 2206–2214.
- title=Vakcína Suchá vakcína proti moru | url=http://www.epidemiolog.ru/catalog_vac/index.php?SECTION_ID=&ELEMENT_ID=476
- Supotnitsky M. V., Supotnitskaya N. S., 2006,
- Supotnitsky M. V., Supotnitskaya N. S., 2006,
- Deng W a kol.. (2002). "". Journal of Bacteriology 184 (16): 4601–4611.
- Parkhill J a kol.. (2001). "". Příroda 413 : 523–527.
- Wagle P.M. (1948). „Nedávné pokroky v léčbě dýmějového moru“. Indian J Med Sci 2 : 489–94.
- Meyer KF. (1950). „Moderní terapie moru“. JAMA 144 : 982–5.
- Kilonzo BS, Makundi RH, Mbise TJ. (1992). „Deset let epidemiologie a kontroly moru v západních horách Usambara, severovýchodní Tanzanie“ . Acta Tropica 50 : 323–9.
- Mwengee W, Butler T, Mgema S, a kol.(2006). „Léčba moru gentamicinem nebo doxycyklinem v randomizované klinické studii v Tanzanii“. Clin Infect Dis 42 : 614–21.
